Chuyên đề Acid trong chương trình Hóa học 9 là một nội dung quan trọng và nền tảng, giúp học sinh có cái nhìn tổng quát về một nhóm chất hóa học phổ biến trong tự nhiên cũng như trong các ứng dụng công nghiệp. Axit không chỉ là một khái niệm xuất hiện trong đời sống hàng ngày mà còn là một thành phần của những phản ứng hóa học quan trọng mà các em sẽ gặp trong suốt quá trình học tập. Qua chuyên đề này, học sinh sẽ được tìm hiểu về khái niệm axit, tính chất hóa học, ứng dụng của axit trong cuộc sống, cũng như các lưu ý về an toàn khi sử dụng axit.
Khái niệm axit và phân loại Axit là một trong những hợp chất hóa học quan trọng, với đặc điểm nổi bật là khả năng giải phóng ion H⁺ khi tan trong nước. Theo định nghĩa hóa học hiện đại, axit là chất có khả năng cho proton (H⁺) hoặc nhận cặp electron tự do từ các phân tử khác nhau. Khi hòa tan trong nước, acid tạo ra dung dịch có tính chất đặc trưng như vị chua, làm đổi màu quỳ tím sang đỏ, và có khả năng dẫn điện tạo ra các ion tự làm. Ví dụ điển hình là các axit vô cơ phổ biến như axit clohydric (HCl), axit sunfuric (H₂SO₄), và axit nitric (HNO₃), những hợp chất học sinh sẽ gặp rất nhiều trong suốt quá trình học tập môn Hóa học. Trong chương trình Hóa học lớp 9, học sinh sẽ được làm quen với các khái niệm cơ bản này thông qua việc phân loại axit dựa trên nhiều tiêu chí khác nhau, chủ yếu là dựa trên cường độ và nguồn gốc của axit. Theo tiêu chí độ mạnh, axit được chia thành hai nhóm chính: **axit mạnh** và **axit yếu**. Axit mạnh, như HCl và H₂SO₄, là những axit có khả năng phân ly hoàn toàn trong dung dịch nước, tức là tất cả các axit phân tử đều giải phóng ion H⁺. Trong khi đó, axit yếu, suy hạn như axit axetic (CH₃COOH) trong ngâm, chỉ phân ly một thành phần trong dung dịch,dẫn đến công việc giải phóng ít ion H⁺ hơn. Việc phân loại này giúp học sinh nắm chắc sự khác biệt về tính chất và khả năng phản ứng của các axit. Ngoài ra, học sinh cũng sẽ tìm hiểu về các axit hữu cơ và axit vô cơ. Axit vô cơ, như HCl, H₂SO₄ và HNO₃, thường được tìm thấy trong các phản ứng hóa học và quá trình công nghiệp. Ngược lại, axit hữu cơ thường xuất hiện trong các hợp chất tự nhiên và sinh học, ví dụ như axit citric (có trong trái cây như cam, chanh) và axit lactic (hình thành trong cơ bắp khi chạy mạnh động). Việc hiểu rõ các loại axit khác nhau giúp học sinh có cái nhìn tổng quát và ứng dụng linh hoạt vào các tình huống thực tế trong và ngoài phòng thí nghiệm.
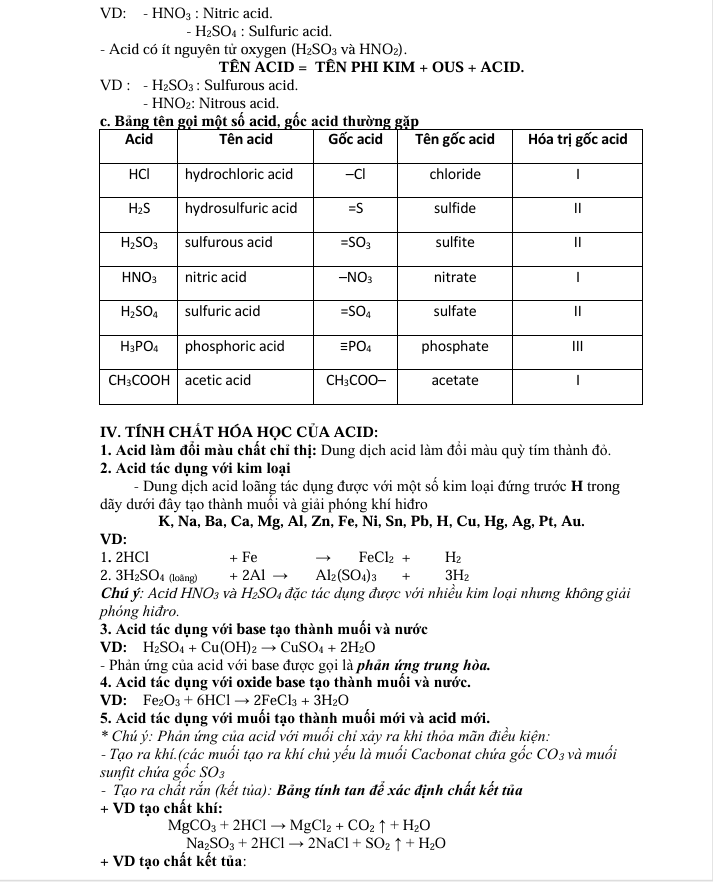
Tính chất hóa học của axit Một trong những phần quan trọng của chủ đề này là tính chất hóa học của axit. Axit có nhiều tính chất hóa học quan trọng mà học sinh cần phải nắm chắc, bao gồm khả năng phản ứng với kim loại, bazơ, oxit bazơ và muối. Đây là những phản ứng thường gặp không chỉ trong phòng thí nghiệm mà còn trong tự nhiên và trong quá trình sản xuất công nghiệp.
Tóm lại, chuyên đề Acid trong Hóa học lớp 9 không chỉ giúp học sinh nắm vững các kiến thức cơ bản về axit, tính chất và ứng dụng của chúng mà còn nâng cao nhận thức về an toàn khi làm việc với hóa chất.